Bez Ozempic: studie ukazuje alternativu ke kontrole obezity u starších lidí
Uprostřed vzestupu farmakologické léčby obezity, kdy léky GLP-1 snižují kalorický příjem, byla obnovena studie z roku 2023, která obnovuje metabolické funkce ztracené stárnutím. dělat opačně.
Na rozdíl od Ozempic, Wegovy nebo jiných per na hubnutí, studie provedená vědci z Cornell University v USA sází na zvýšení energetického výdeje vyřešením jedné z největších záhad medicíny: Proč s přibývajícím věkem ztrácíme schopnost spalovat tuky?
Výzkum zjistil, jak zvrátit proces charakteristický pro stárnutí, při kterém speciální buňky kolem krevních cév produkují nadbytek proteinu (Pdgfrβ), který blokuje tvorbu béžového tuku, tkáně, která obvykle spaluje kalorie a vytváří teplo.
Jinými slovy, práce identifikuje specifický a farmakologicky životaschopný mechanismus schopné obnovit termogenní kapacitu, kterou ztrácíme stárnutím. Objev nabízí možnost nových terapií proti obezitě, zejména u starší populace.
Přestože působí zcela opačnými cestami (léky GLP-1 regulující příjem energie a protein Pdgfrβ stimulující výdej energie), mají tyto mechanismy synergický potenciál, protože případná kombinace těchto dvou by v těle vytvořila dvojnásobný kalorický deficit.
Pochopení tří typů tělesného tuku
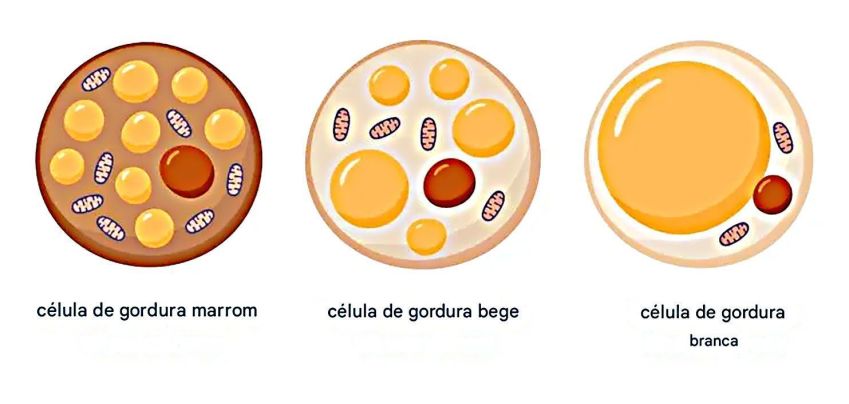
Když mluvíme o tělesném tuku, máme na mysli především dva typy tukové tkáně – bílou (TAB) a hnědou (TAM). První hlavní funkcí je ukládat energii, zatímco BAT spaluje energii k výrobě tepla a regulaci tělesné teploty (termogeneze).
Počínaje rokem 2008 výzkum odhalil existenci třetího typu buněk, které tvoří tuk v těle, rozptýlený mezi usazeniny bílé tukové tkáně. Protože měl schopnost získat vlastnosti TAM, byl adipocyt nazýván béžovou tukovou tkání.
TABg, který se normálně spouští delším vystavením chladu, funguje jako termogenní buňka který spaluje kalorie v ložiscích bílého tuku. K tomu snižuje hladinu cukru v krvi a odbourává mastné kyseliny, které způsobují kornatění tepen a srdeční choroby.
Jak stárneme, reakce na chlad se drasticky snižuje, takže tělo upřednostňuje produkci bílého tuku. Systém postupně ztrácí schopnost tvořit tyto buňky spalující energii, což přispívá k metabolickému poklesu charakteristickému pro stáří.
To znamená, že ačkoli u mladých lidí dochází k sezónním změnám v béžovém tuku, „starší člověk by musel stát venku ve sněhu ve spodním prádle, aby získal stejné termogenní účinky,“ vtipkuje spoluautor Daniel Berry, profesor v Divize nutričních věd, v prohlášení zveřejněném v době studie.
Biochemie tuku ve stárnutí
Pro hlavní autorku studie, Abigail Benvie, bylo konečným cílem výzkumu odpovědět na otázku: „Aniž bychom museli lidi vystavovat chladu po delší dobu, existují metabolické cesty, které můžeme stimulovat a které by mohly mít stejný účinek?“
Poté, co identifikovali Pdgfrβ jako jakousi „molekulární brzdu“, která brání přeměně speciálních buněk kolem cév na béžový tuk, použili léky imatinib (schválený pro leukémii) a SU16f k zablokování účinku proteinu u starších myší na pět dní.
Myši, které byly léčeny blokátory Pdgfrp, byly vystaveny chladu po dobu jednoho týdne. Překvapivě, stará zvířata znovu získala potenciál tvořit béžový tukfunkci, kterou přirozeně ztratili s postupujícím stárnutím.
Mechanismus funguje prostřednictvím molekulární kaskády: blokování Pdgfrβ zvyšuje produkci IL-33, látky, která aktivuje speciální imunitní buňky. Tyto lymfocyty pak stimulují transformaci progenitorových buněk na skutečné „buněčné pece“ spalující energii.
Poté, co stárnoucí myši začaly spalovat energii jako mladé, novější práce naznačují, že obrácení signalizace také reaktivuje imunitní buňky, které jsou nezbytné pro udržení této tkáně. Ve spojení se stejným procesem byly identifikovány nové molekuly související s béžovým tukem.
V současném kontextu lze směr výzkumu, který zvyšuje spalování energie v samotné tukové tkáni, prozkoumat jako účinnou léčbu pro starší lidi, u kterých pokles termogeneze béžových a hnědých tuků ztěžuje kontrolu hmotnosti.




